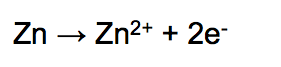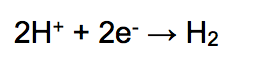Meyve ve Sebze Pili Tasarlayalım
Deneyler köşesinin bu etkinliğinde meyve ve sebzeleri kullanarak kendi pilimizi tasarlıyoruz.
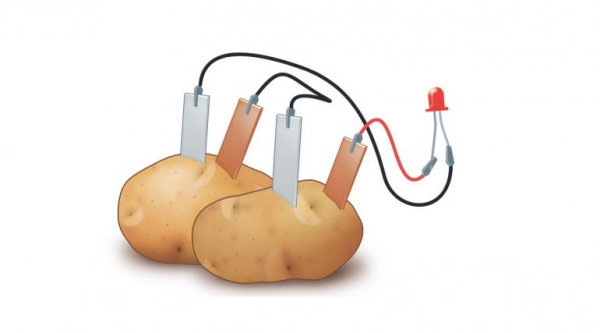
Deneyler köşesinin bu etkinliğinde patates kullanarak yapacağımız pil ile bir LED’i yakmaya çalışıyoruz. Kolayca bulabileceğiniz malzemelerle evde ve okulda gerçekleştirebileceğiniz bu etkinlik sayesinde siz de meyve ve sebzeleri kullanarak kendi pilinizi tasarlayabilirsiniz.
Anahtar kavramlar: Elektrik, pil, kimyasal enerji
Bilmekte fayda var!
Piller olmasaydı hayatımız nasıl değişirdi?
Piller elektrik enerjisinin kimyasal enerji şeklinde depolandığı cihazlardır. Eğer piller olmasaydı birçok taşınabilir elektronik cihaz (örneğin tabletler, telefonlar, saatler, işitme cihazları, kalp pilleri) hayatımızda olmazdı.
Bir kimyasal tepkime gerçekleşirken enerji açığa çıkabilir ya da kimyasal tepkimenin gerçekleşmesi için enerjiye ihtiyaç duyulabilir. Örneğin kömürün oksijenle tepkimesi yani yanması sonucu ısı enerjisi açığa çıkar.
Pillerde gerçekleşen tepkime sonucu ise elektrik enerjisi açığa çıkar. Tekrar doldurulabilir piller şarj edilirken bu sürecin tersi gerçekleşir. Bu tür tepkimeler elektrokimyasal tepkimeler olarak isimlendirilir. Elektrokimyasal tepkimede yer alan maddelerden biri elektron alarak indirgenirken, diğeri elektron vererek yükseltgenir. Bir elektrokimyasal tepkimenin oluşabilmesi için indirgenme ve yükseltgenme süreçlerinin birlikte gerçekleşmesi gerekir.
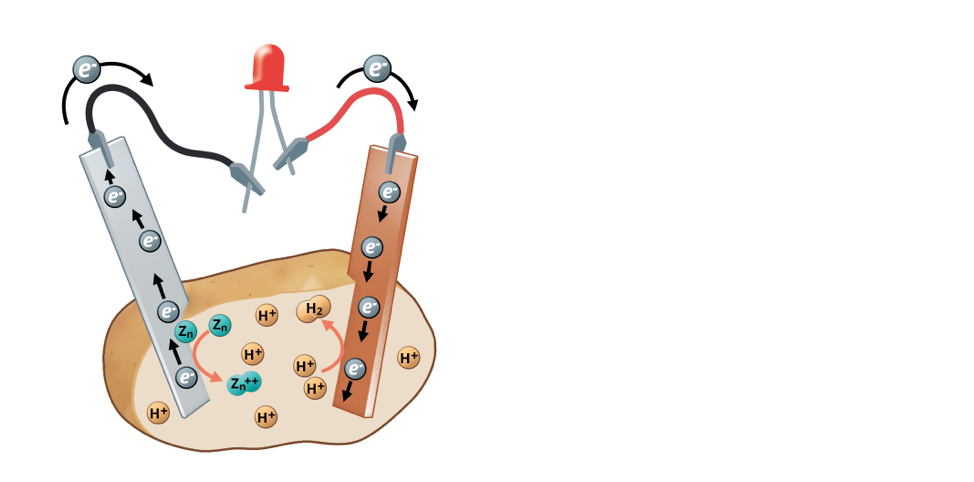
Elektrokimyasal tepkimenin gerçekleştiği sistem elektrokimyasal hücre olarak isimlendirilir. Bu sistem iki elektrot (anot ve katot) ve elektrolit olarak isimlendirilen bir çözeltiden oluşur.
Elektrokimyasal tepkime sonucu elektrik akımının oluşabilmesi için elektrotlar arasında iletkenliğin sağlanması gerekir. Elektrotlar arasındaki elektriği iletebilen bağlantı kabloları ve elektrolit çözeltisi elektrik yüklerinin taşınmasını sağlar.
Bu tepkimede neden çinkonun yükseltgenip neden bakırın indirgendiği sorusu aklınıza gelebilir. Bu sorunun cevabı kimya derslerinden hatırlayabileceğiniz “elektronegatiflik” kavramında saklı.
Bakırın elektronegatifliği yani elektronları çekme isteği çinkonunkinden yüksektir. Bu nedenle yukarıdaki elektrokimyasal hücrede çinko yükseltgenirken bakır indirgenir ve sonuçta elektrik akımı oluşur.
Pilin içinde gerçekleşen elektrokimyasal tepkime sonucu elektrik akımının oluşabilmesi için elektronların sistemin bir ucundan diğerine ulaşması gerekir. Elektronların izlediği bu yola elektrik devresi denir. Tepkimenin gerçekleşmesini sağlayan maddeler tükendiğinde kimyasal tepkime durur ve pil boşalır.
Farklı pil türleri vardır. Örneğin kumandalarda, oyuncaklarda ya da duvar saatlerinde alkalin piller kullanılırken, cep telefonlarının bataryaları lityum iyon pillerden üretilir.
Deneyler köşesinin bu etkinliğinde patates kullanarak bir pil yapacak ve bu pil ile bir LED’i yakmaya çalışacağız. Bu etkinliği hayal gücünüzden ilham alarak limon, domates, elma, portakal gibi farklı meyve ve sebzelerle deneyebilir ve elde ettiğiniz sonuçları karşılaştırabilirsiniz.
Nelere ihtiyacımız var?

- 3 adet LED
- 3 adet bakır levha
- 3 adet çinko levha
- 5 adet bağlantı kablosu (krokodil kablo)
- 3 adet patates
- Multimetre
Multimetre elektrik akımını, potansiyelini ve direncini ölçebilen bir cihazdır.
Ne yapıyoruz?

1. Bir çinko ve bir bakır levhayı patatese batıralım. Elektrotların bir kısmı patatesin içine girmeli bir kısmı dışarıda kalmalıdır.
2. Krokodil kablonun bir ucunu patatese batırdığımız bakır levhaya, diğer ucunu ise multimetrenin artı ucundan çıkan kabloya bağlayalım.
3. Diğer krokodil kablonun bir ucunu patatese batırdığımız çinko levhaya, diğer ucunu ise multimetrenin eksi ucundan çıkan kabloya bağlayalım.
4. Hazırladığımız patates pilinin elektrik potansiyelini multimetre yardımıyla ölçelim ve ölçtüğümüz değeri not edelim.
5. Krokodil kabloların multimetreden çıkan kablolara bağlı uçlarını ayıralım.
6. Çinko elektrota bağlı kablonun diğer ucunu LED’in kısa bacağına, bakır elektrota bağlı kablonun diğer ucunu LED’in uzun bacağına bağlayalım. LED yandı mı?
LED yanmadıysa daha fazla sayıda patates kullanarak yeni bir pil hazırlayalım.
7. Bunun için diğer iki patatesin her birine bir çinko ve bir bakır levha batıralım.
8. Krokodil kabloların bir ucunu patatese batırdığımız bakır levhaya, diğer ucunu ise multimetrenin artı ucundan çıkan kabloya bağlayalım.
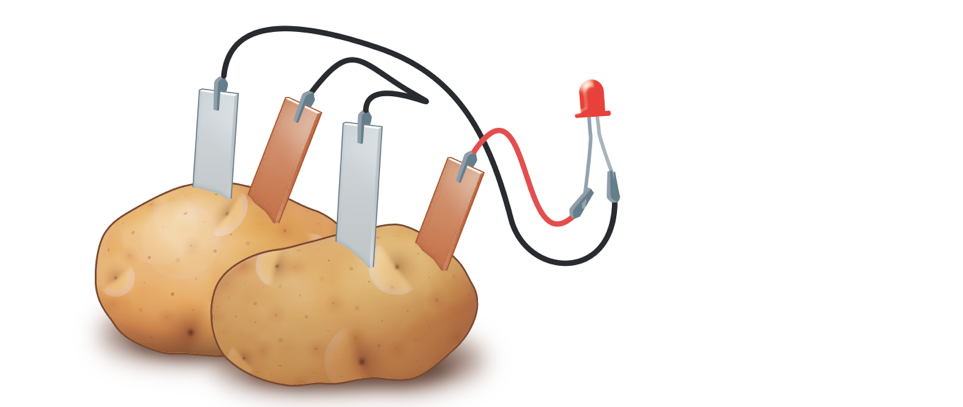
9. Diğer krokodil kablonun bir ucunu bu patatese batırdığımız çinko levhaya, diğer ucunu ikinci patatese batırdığımız bakır levhaya bağlayalım.
10. Başka bir krokodil kabloyu ikinci patatese batırdığımız çinko levhaya, diğer ucunu ise multimetrenin eksi ucundan çıkan kabloya bağlayalım.

Bu şekilde patatesleri seri bağlayarak bir pil hazırladık.
11. Hazırladığımız iki patatesten oluşan pilin elektrik potansiyelini multimetre yardımıyla ölçelim ve ölçtüğümüz değeri not edelim.
12. Krokodil kablonun multimetrenin artı ucundan çıkan kabloya bağlı ucunu ayırıp LED’in uzun bacağına, eksi ucundan çıkan kabloya bağlı ucunu ayırıp LED’in kısa bacağına bağlayalım. LED şimdi yandı mı?
Uyarı: Pil olarak kullandıktan sonra meyve ve sebzeleri yemeyin.
Ne oldu?
Patatesin içinde asit özelliği gösteren maddeler var. Bu maddeler patatesteki suyun içinde çözünür. Bu nedenle patatesin içindeki suda artı yüklü hidrojen iyonları bulunur ve patatesteki su elektrokimyasal hücrelerdeki elektrolit çözeltisinin işlevini görür. Taze patatesler daha fazla su içerdiği için elektrik potansiyelleri daha yüksektir.
Hazırladığımız patates pilinde patatese batırdığımız çinko (çinko elementinin kimyasal simgesi Zn’dir) elektrottaki çinko atomları iki elektron vererek yükseltgenir ve artı yüklü çinko iyonları oluşur.
Açığa çıkan elektronlar elektrik devresinden akarak bakır elektrota ulaşır. Bakır elektrotun etrafındaki artı yüklü hidrojen iyonları (H+) ise elektron alır ve hidrojen molekülü (H2) oluşur.
LED’ler (ışık yayan diyotlar) telefon, bilgisayar ve televizyon ekranlarının yanı sıra ev, ofis ve şehir aydınlatmalarında da sıkça kullanılır. LED’lerin bacaklarının uzunluklarının birbirinden farklı olduğuna dikkat etmişsinizdir. LED’ler elektrik akımını tek yönde iletir. Bu nedenle LED’lerin uzun bacağını pilin (+) kutbuna, kısa bacağı ise (-) kutbuna bağladık. Tersi durumda LED yanmazdı.
Düşünelim!
Patates pilimiz ile LED ne kadar süre yandı?
Patates pilimiz ile multimetrede ölçtüğümüz değeri hangi faktörler etkileyebilir?
Patatesi suda bekletirsek patates pilimiz ile multimetrede ölçtüğümüz değer değişir mi?
Pil yapımında elektrot olarak bakır ve çinkodan başka hangi metalleri kullanabiliriz?
Pil yapımında başka hangi meyveler ve sebzeler kullanılabilir?
-
Bushway, R., Bureau, J., McGann, “Determination of organic acids in potatoes by high performance liquid chromatography”, Journal of Food Science,Cilt 49, Sayı 1, s. 76-77, 1984.