Maddeler Nasıl Çözünür?
Çayın içinde şekerin ya da gazlı içeceklerde basınçlı karbondioksitin çözünmesi günlük hayatta en sık karşılaştığımız çözünme örneklerinden bazıları. Peki çözünme olayının nasıl gerçekleştiğini hiç merak ettiniz mi?

Marina Bagrova / iStock
İki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasıyla oluşan karışımlara çözelti diyoruz. Çözelti; çözücü ve çözünen adı verilen iki unsurdan oluşur. Çözeltideki miktarca az olan madde çözünen, çok olan madde ise çözücüdür. Çözünme olayı gerçekleşirken çözünen madde, iyonlarına ya da moleküllerine ayrılır. Çözünme olayı sırasında çözünen maddenin her iyonu ya da molekülü çözücü maddenin molekülleri tarafından çevrelenir.
Çözücü madde ile çözünen maddenin tanecikleri arasındaki çekim kuvveti çözünen maddenin kendi tanecikleri arasındaki çekim kuvvetinden güçlü olduğunda çözünme olayı gerçekleşir. Örneğin su (çözücü) ve tuz (çözünen) tanecikleri arasında iyon-dipol etkileşimi olarak isimlendirilen bir etkileşim kuvveti vardır. Bu etkileşim kuvveti tuzu oluşturan artı yüklü sodyum iyonları ile eksi yüklü klor iyonları arasındaki elektrostatik çekim kuvvetinden güçlü olduğundan tuz, suda çözünebilir.
Tüm Maddeler Birbiri İçerisinde Çözünebilir mi?
Maddeler bir araya geldiğinde bu maddeleri oluşturan iyonlar ve moleküller gibi kimyasal türler arasında bazı etkileşimler oluşur. Bir maddenin diğer bir madde içerisinde çözünebilmesi için kimyasal türler arasındaki bu etkileşimlerin benzer olması gerekir. Bu durumu “Benzer Benzeri Çözer” ilkesi olarak adlandırıyoruz.

Azulillo / iStock
Zeytinyağı apolar, su ise polar yapıda olduğu için birbiri içerisinde çözünmez.
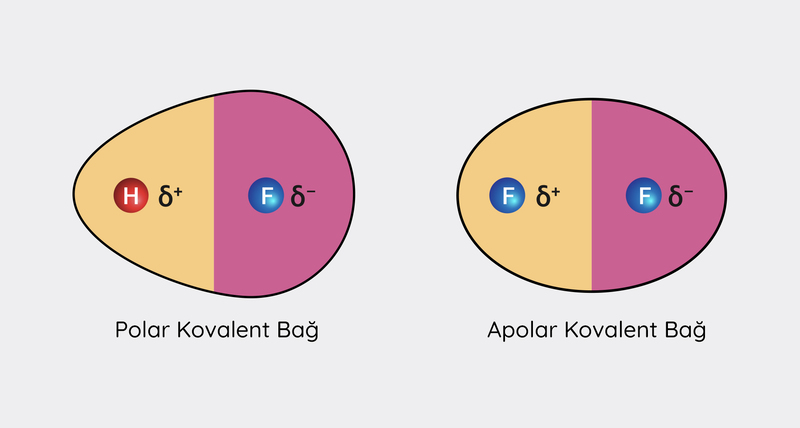
Yapısı benzer maddeler birbiri içinde çözünebilir. Buna göre polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde iyi çözünür. Bir maddenin polarlığı o maddenin moleküllerini oluşturan atomların elektronegatifliklerinden yani bağ oluşumuna katılan elektronlarını çekebilme gücündeki farktan kaynaklanır. Bu fark, elektronegatifliği yüksek atomun kısmen eksi yükle (𝛿-) yüklenmesine, diğer atomun ise kısmen artı yükle (𝛿+) yüklenmesine sebep olur. Apolar yapıda bir maddenin moleküllerinde ise pozitif veya negatif kutuplar oluşmaz çünkü apolar bir molekülde artı (+) ve eksi (-) yükler molekül boyunca eşit olarak dağılmıştır.
Jonas Reuel / iStock
Moleküller arası çekim, polar yapıdaki bileşiklerde bir molekülün negatif yüklü kısmı diğer molekülün pozitif yüklü kısmı tarafından çekildiğinden, son derece kuvvetlidir. Bu nedenle bileşiğin bütün molekülleri arasında bir ağ yapısı oluşur. Apolar bir molekül ise polar bir moleküldeki bu ağ yapısını bozamaz. Bundan dolayı polar bir madde, apolar bir madde içerisinde çözünemez. Örneğin karbontetraklorür (CCl4), apolar bir moleküldür ve polar bir molekül olan suda çözünemez. Çünkü su molekülleri arasındaki çekim kuvveti, karbontetraklorür ile su molekülü arasındaki çekim kuvvetinden çok daha fazladır.
Atomik Düzeyde Çözünme Olayı
Çözünme olayı, çözücü ve çözünenin etkileşime girdiği ve bu ikisi arasındaki etkileşimin durmadan devam ettiği karmaşık bir süreçtir. Çözünme olayının başlangıcında çözücü madde taneciklerinin nasıl davrandığı yıllardır merak edilen bir konuydu. Yakın zamanda yapılan bir çalışmada araştırmacılar, çözünme sürecinin atomik düzeyde nasıl gerçekleştiğini görüntülemeyi başardı.

Frentusha / iStock
Sonuçları Nature dergisinde yayımlanan çalışmada, -255 °C'ye soğutulmuş bir sıvı helyum damlasının içine önce tek bir ksenon atomu hapsedildi. Ardından damlanın dış kenarına tek bir sodyum atomu eklendi. Araştırmacılar sodyum atomunu pozitif yüklü bir iyona dönüştürmek için atoma kısa bir lazer atımı gönderdi. Bunun sonucunda helyum atomları sodyum iyonuna yapışmaya başladı. Böylece çözünme olayı başladı.
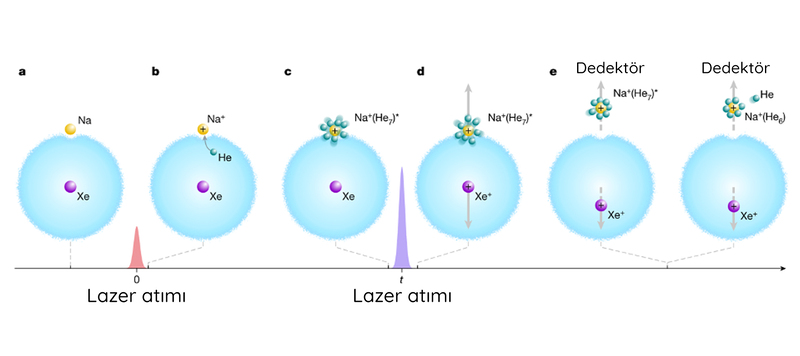
Araştırmacılar ksenon atomuna daha sonra başka bir lazer atımı göndererek atomu pozitif yüklü bir iyona dönüştürdü. Sodyum ve ksenon iyonları birbirini o kadar itti ki sodyum iyonu, bağlı olduğu helyum atomlarıyla birlikte damlacıktan bir dedektöre itildi. Böylece anlık görüntüler elde edilmiş oldu.
Birden fazla ve ardışık olarak eş anlı görüntü elde ettikten sonra bunları birleştirerek çözünme sürecini gösteren bir film oluşturdular. Böylece çözünme olayının atomik düzeyde nasıl gerçekleştiği daha yakından anlaşılmış oldu.
Kaynaklar:
- 15.4: Solute and Solvent - Chemistry LibreTexts
- https://www.thoughtco.com/definition-of-nonpolar-molecule-604582
- https://dx.doi.org/10.1038/d41586-023-02950-6
- Solutions, Solvation, and Dissociation - Chemistry LibreTexts
- 13.2: Solutions - Homogeneous Mixtures - Chemistry LibreTexts
- https://www.acs.org/education/resources/k-8/inquiryinaction/fifth-grade/chapter-1-investigating-matter-at-the-particle-level/lesson-1-3--dissolving-and-back-again.html
- 15.2: Why do Ionic Solids Dissolve in Water (Ion-Dipole IMF)?