Alkali Metal Tepkime Deneyi
Metallerin su ile tepkimeye girdiklerinde bazılarının çok hızlı ve şiddetli bazılarının ise yavaş ya da hiç tepkime vermemesinin nedenini hiç düşündünüz mü? Bu etkinlikte, alkali metallerin suyla tepkimelerini karşılaştırarak periyodik tabloda atom numarasının ve atom yapısının tepkime davranışını nasıl etkilediğini gözlemleyebilirsiniz.

Pla2na/iStockphoto.com
Alkali metalleri kısaca tanıyalım
Periyodik tablo, elementlerin özelliklerini anlamamızı sağlayan temel bilimsel araçlardan biridir. Bu tablonun oluşum sürecinde Antoine-Laurent de Lavoisier, Johann Wolfgang Döbereiner, John Alexander Reina Newlands, Julius Lothar Meyer gibi birçok bilim insanının önemli katkıları olmuştur. Günümüzde kullandığımız tabloya en yakın sistemi ortaya koyan bilim insanı ise Dimitri Mendeleyev’dir. Mendeleyev, elementleri atom kütlelerine göre sıralamış ve elementlerin özelliklerinin belirli aralıklarla yani periyodik olarak tekrarlandığını fark etmiştir. Ancak bazı elementlerin bu düzene tam uymaması, yeni bir ölçüt gerektiğini göstermiştir. Daha sonra Henry Gwyn Jeffreys Moseley, elementleri atom numaralarına göre sıralayarak bu sorunu çözmüş ve modern periyodik tablonun temelini atmıştır.
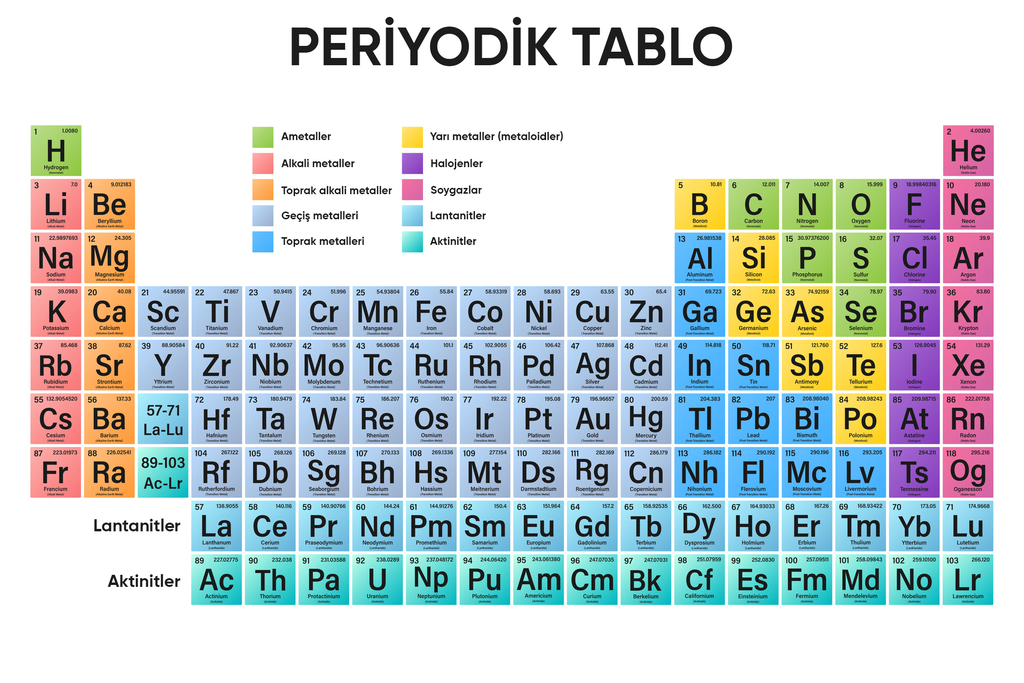
Periyodik tabloda gruplar iki farklı şekilde adlandırılır: Harf ve sayıların kullanıldığı sistem (1A, 2A gibi) ve Uluslararası Temel ve Uygulamalı Kimya Birliği’nin kabul ettiği numaralandırma sistemi (1. grup, 2. grup gibi). Bu gruplar, içerdikleri elementlerin benzer özelliklerine göre isimlendirilir. Örneğin 1A grubunun adı alkali metallerdir.
Yevhen Borysov/gettyimages.com
Periyodik tablonun ilk sütunundaki elementlerin oluşturduğu grup, 1A grubudur.
Bu grupta hidrojen (H), lityum (Li), sodyum (Na), potasyum (K), rubidyum (Rb), sezyum (Cs) ve fransiyum (Fr) elementleri yer alır. Hidrojen ametal özellik gösterirken diğer elementler metaldir. Bu gruptaki metaller oluşturdukları bileşiklerde genellikle +1 değerlikli iyon oluşturur. Hidrojen ise istisnai davranarak ametallerle oluşturduğu bileşiklerde +1, metallerle oluşturduğu bileşiklerde -1 değerlik alabilir.
Metal grupları arasında 1A grubu elementleri (alkali metaller), en dış enerji düzeylerinde yalnızca 1 elektron bulundurmaları ve düşük iyonlaşma enerjileri nedeniyle elektron vermeye en yatkın metaller arasındadır. Bu nedenle periyodik tablonun tepkimeye girme eğilimi en yüksek metal grubunu oluştururlar. Suyla temas ettiklerinde şiddetli tepkimeye girerler. Parlak yüzeye sahip olan bu elementler ısı ve elektriği iyi iletir. Ayrıca yoğunlukları ve erime noktaları diğer birçok metale göre düşüktür.

andriano_cz/iStockphoto.com
Alkali metallerin ve oluşturdukları bileşiklerin büyük bir kısmı farklı alanlarda yaygın olarak kullanılır. Saf hâlde en dikkat çekici uygulamalardan biri, rubidyum ve sezyum elementlerinin atom saatlerinde kullanılmasıdır. Özellikle sezyum atom saatleri, saniyenin tanımlanmasında temel alınır. Yumuşak ve kolay işlenebilir bir alkali metal olan sodyumun bileşikleri ise sodyum buhar lambaları gibi aydınlatma sistemlerinde kullanılır. Lityum, ilaç yapımında ve lityum iyon pillerde önemli bir bileşen olarak değerlendirilir. Sodyum ve potasyum, biyolojik sistemlerde elektrolit olarak kritik roller üstlenirken diğer alkali metaller insan vücudu için temel elementler arasında yer almaz ve toksik etki gösterebilir. Sofra tuzu olarak bilinen sodyum klorür ise antik çağlardan bu yana kullanılan önemli bir bileşiktir.
Alkali metaller su ile tepkimeye girer. Bu tepkimenin şiddeti; tepkimenin daha hızlı gerçekleşmesi, daha fazla ısı açığa çıkması ve daha belirgin gaz çıkışı gibi durumlarla kendini gösterir. Tepkimenin şiddeti, periyodik tabloda yukarıdan aşağı doğru gidildikçe artar. Bu değişimin temel nedeni, grup içinde aşağı inildikçe atom yarıçapının artması ve değerlik elektronunun çekirdeğe daha zayıf bağlanmasıdır. Bu durum, elektronun kopmasını kolaylaştırır. Alkali metaller suyla tepkimeye girerken bir elektron vererek iyonlaştıklarından bu tepkimeler diğer birçok metal grubuna kıyasla daha hızlı ve şiddetli gerçekleşir.
Deneyin amacı nedir?
Doğada bileşik hâlde bulunan alkali metallerin su ile tepkimesi oldukça şiddetlidir. Bu elementler su ile tepkimeye girerek hidrojen gazı (H2) açığa çıkarır ve çözelti ortamında kuvvetli bazlar oluşturur. Bu deneyin amacı, bu tepkimelerin şiddetini ve tepkime sonucunda oluşan maddeleri gözlemlemektir.
Alkali metal tepkime simülasyonunu tanıyalım
Bu deneyde, ekranın sol tarafında verilen alkali metaller ekranın ortasında bulunan suya eklendiğinde oluşan tepkimeyi ve tepkime şiddetini gözlemleyebilirsiniz. Ekranın sağ tarafında ise oluşan alev rengi, ortaya çıkan ürünler ve kimyasal denklem gibi tepkimeye ait bilgileri inceleyebilirsiniz.
Düşünelim
Alkali metallerin (1A grubu) suyla tepkimeye girerek H₂ gazı ve kuvvetli bir baz oluşturduğunu ve bu tepkimenin periyodik tabloda aşağı inildikçe şiddetlendiğini öğrendik.
Peki aynı deneyi bu kez 1A grubu yerine 2A grubundan bir metal (örneğin magnezyum ya da kalsiyum) ile yapsaydık:
- Tepkimenin hızı ve şiddeti nasıl olurdu?
- Ortaya çıkan ürünler neler olurdu?
- Grup içinde aşağı inildikçe nasıl bir değişim gözlemlenirdi?
Kaynak:
Yazar Hakkında: Elif Gürbüz Poyraz ODTÜ Fen Bilgisi Eğitimi Doktora Öğrencisi