Evrenin Yapı Taşlarını Sınıflandırmak
Bir periyodik tabloda elementler yapısal özelliklerine göre kategorilere ayrılarak sınıflandırılır. Fakat periyodik tablonun nasıl okunacağı yani periyodik tablodan neler öğrenebileceğimiz bazı önemli fizik kurallarına bağlıdır.

Bir periyodik tabloda elementler yapısal özelliklerine göre kategorilere ayrılarak sınıflandırılır. Fakat periyodik tablonun nasıl okunacağı yani periyodik tablodan neler öğrenebileceğimiz bazı önemli fizik kurallarına bağlıdır. Şüphesiz ki aralarındaki benzerlikler nedeniyle aynı satır ve sütunlara yerleştirilen elementlerden oluşmuş böyle bir tabloyu geliştirilme fikri birdenbire ortaya çıkmadı. Gelin, yaşadığımız evreni ve günümüz teknolojisini şekillendiren elementlerin ve özelliklerinin keşfedilme serüvenine birlikte göz atalım.
Üniversite öğrencilerine vereceği kimya derslerinde faydalı olacağı düşüncesi ile bir kitap yazma kararı alan Dimitri Mendeleyev’in bu serüvende önemli rolü var. Mendeleyev’in 19. yüzyılın son çeyreğinde bitirdiği kitabının birinci cildinde o zamana kadar bilinen 63 elementin 8’inin özelliklerine ait bilgiler yer alıyordu. Geriye kalan 55 element ise kendilerine kitabın ikinci cildinde yer bulabildi. Kitapta her bir element için sayfalar dolusu bilgi bulunduğundan Mendeleyev’in derlediği bu bilgileri bir kural dâhilinde yeniden düzenlemesi gerekti.
Peki, Evrenin Yapı Taşları İçin Uygulanabilecek Basit ve Anlaşılır Bir Sınıflandırma Geliştirilebilir mi?
Mendeleyev başlangıçta elementleri atom ağırlıkları ve kimyasal özelliklerine göre sınıflandırmıştı. 17 Şubat 1869’da (Jülyen takvimine göre) 63 elementi içeren bir tabloyu, yayınladığı bilimsel makale sayesinde bilim dünyasına sundu. Tüm zamanların en önemli bilimsel katkıları arasında yer alan bu gelişmenin 150. yılı olması nedeniyle 2019 yılı Birleşmiş Milletler tarafından Uluslararası Kimyasal Elementlerin Periyodik Tablosu Yılı olarak ilan edildi.
Rus kimyacı Dimitri Mendeleyev laboratuvarında çalışıyor.
Kimyacı John Dalton da Mendeleyev’den önce elementleri sınıflandırmak için bir tablo oluşturmak amacıyla çalışmalar gerçekleştirmişti. Mendeleyev’in tablosunu kendisinden önce gerçekleştirilmiş çalışmalardan ayıran en önemli özelliği, oluşturulan tabloda bilinen tüm elementlere yer verilmiş olması.
1860’lı yıllarda elementlerin birçoğunun atom ağırlıkları bilinmiyordu. Aslında o yıllarda atomun yapısı henüz tam olarak anlaşılamamıştı. Atomun yapı taşları olan proton, nötron ve elektron henüz keşfedilmemişti. Örneğin elektron 1897’de Joseph John Thomson tarafından keşfedildi.
Mendeleyev atom ağırlıkları bilinmeyen elementler için tahminî bir atom ağırlığı belirledi. Ayrıca o dönemde henüz keşfedilmemiş elementlerin periyodik tablodaki yerlerini ve özelliklerini de tahmin etti.
Günümüzde ise periyodik tablodaki elementler artan atom numaralarına (atom çekirdeğindeki proton sayısı) göre sıralanır. Atom çekirdeği etrafında belirli enerji seviyelerindeki yörüngelerde bulunan elektronların hareketleri üzerine temellendirilmiş bu yeni sıralamanın temelleri, kuantum kuramının da mimarları arasında yer alan Niels Bohr tarafından atıldı.
Değişim İçin Hazır mısınız?
Periyodik tablonun 18. grubunda yer alan soygazlar tepkimeye girme konusunda isteksiz olmalarıyla bilinir. Ancak bugün soygazları oluşturan elementlerden bazılarının nadiren başka bir element ile tepkimeye girebildiğini biliyoruz. İlginçlikler bununla da sınırlı değil. Periyodik tablonun 12. gurubunda yer alan çinko (Zn) ve kadmiyum (Cd) oda sıcaklığında katı iken aynı gurupta yer alan cıva (Hg) oda sıcaklığında sıvı halde bulunur. Ayrıca periyodik tablonun altında yer alan f bloğunu oluşturan elementlerin (lantinitler ve aktinitler) nasıl yerleştirilmesi gerektiğiyle ilgili farklı görüşler var. Bu nedenlerle günümüzde elementlerin nasıl daha iyi bir biçimde sınıflandırılabileceği tartışma konusu. Bazı bilim insanları periyodik tablo için değişimin gerekli olduğunu düşünüyor.
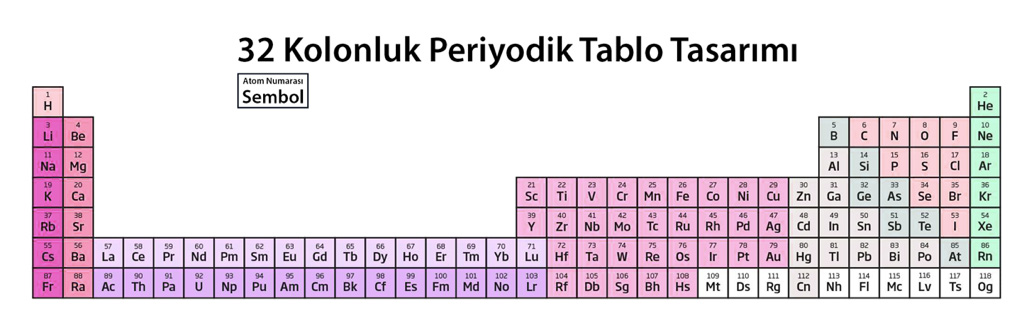
Önerilerden biri elementlerin atom numaralarına göre kesintisiz bir şekilde dizilimini mümkün kılan, 32 kolondan oluşan bir periyodik tablo. Böylece f bloğu elementleri periyodik tablonun altında ayrı bir bölümde değil tablonun içinde yer alabiliyor.
Los Angeles’taki Kaliforniya Üniversitesi’nden Eric Scerri’nin önerdiği, 32 kolondan oluşan periyodik tablo
En son keşfedilen elementler atom numaralarına göre periyodik tabloya yerleştirildi. Ancak örneğin atom numarası 117 olan ve 17. grupta yer alan tennessinin (Ts) halojenlerle, atom numarası 118 olan ve 18. grupta yer alan oganessonun (Og) soygazlarla benzer özellikler gösterip göstermediği henüz bilinmiyor. Ayrıca bundan sonra keşfedilecek elementlerin periyodik tabloya nasıl yerleştirileceği de başka bir soru.
Kaynaklar:
- Fontani, M., Costa, M., Orna, M. V., The Lost Elements: The Periodic Table’s Shadow Side, Oxford University Press, 2015.
- D. I. Mendeleev and His Contributions to the World Science Conference, 2009.
- Scerri, E. R., The Periodic Table: its Story and its Significance, Oxford University Press, 2006.
- Brock, W. H., The Fontana History of Chemistry, Fontana Press, 1993.