Asit ve Baz Nedir?
Limon suyu ekşidir. Elimizi yıkamak için kullandığımız sabun ise kaygandır. Bu maddeler sırasıyla asit ve baz olarak sınıflandırılır. Peki, asit ve baz nedir? Okulda kimya dersinde ya da laboratuvarında sıkça karşılaştığımız bu kavramlar neden önemli?

BlackMagic / iStock
Asitler ve bazlar hayatımızın her alanında karşılaştığımız maddeler. Örneğin asit yağmurları önemli bir çevre sorunudur. Tükettiğimiz besinlerin sindirilmesinde önemli rolü olan mide öz suyu asittir. Çamaşırları ve bulaşıkları yıkarken kullandığımız deterjanlar ise bazik özelliktedir.

D-Keine / iStock
Asit, ekşi anlamına gelen Latince acidus kelimesinden türetilmiş. Bu nedenle ekşi tadı olan yiyecekler çoğunlukla asit özelliği gösterir.
Asit ve baz kavramları maddelerin kimyasal tepkimelerde nasıl davranacağı hakkında bilgi verir. İlk olarak “Asit ve baz nedir?” sorusunu cevaplayalım.
Bu kavramlar için yapılan birden fazla tanım var. Bunlar arasında en yaygın kullanılanlardan biri İsveçli bilim insanı Svante Arrhenius tarafından yapılan Arrhenius asit-baz tanımı. Buna göre suda çözündüğünde çözeltiye hidronyum (H3O+) veren maddelere asit, hidroksil (OH-) iyonu veren maddeler baz denir.
pikepicture / iStock
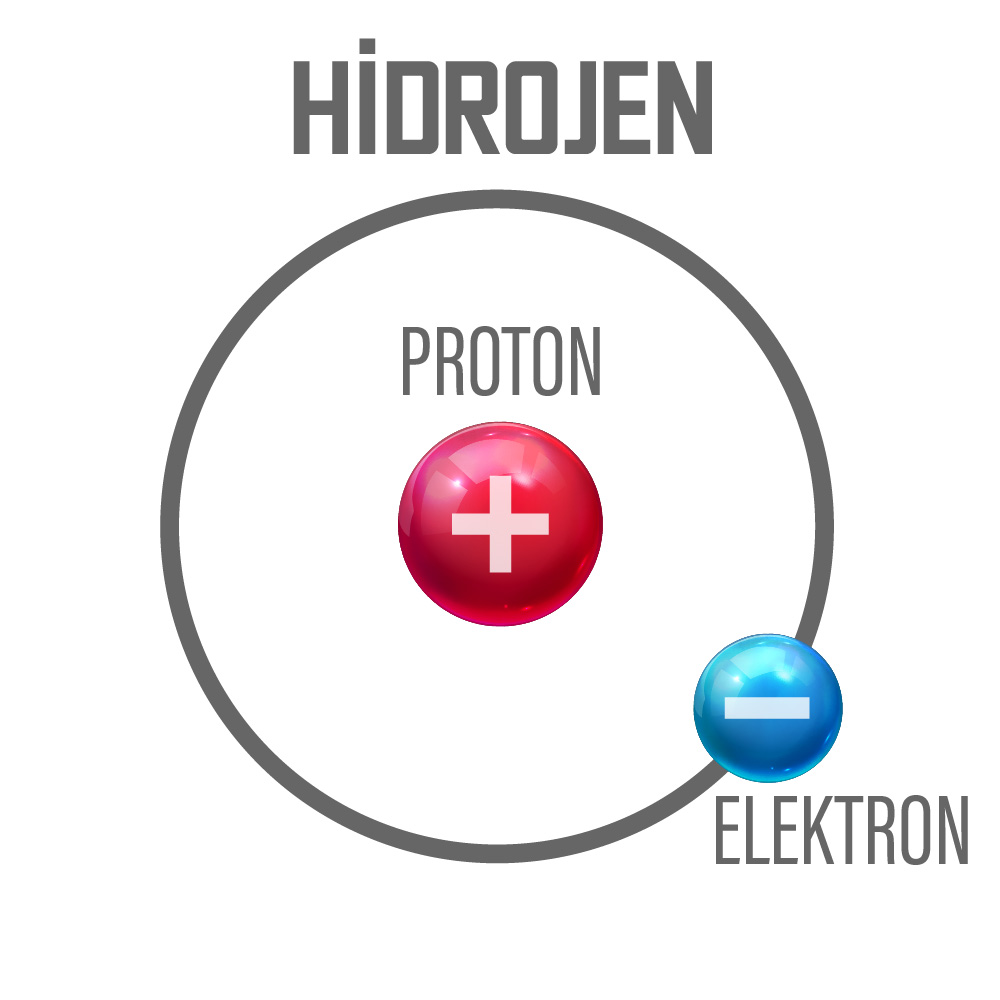
Bir proton ve bir elektrona sahip hidrojen atomu bir elektron verdiğinde artı yüklü hidrojen iyonu oluşur.
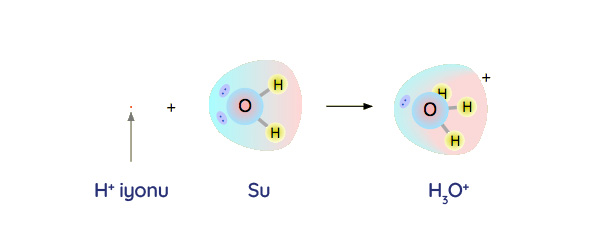
Tepkimeye girme istediği son derece yüksek olan artı yüklü hidrojen, çevredeki su (H2O) molekülleri ile tepkimeye girerek hidronyum (H3O+) iyonunu oluşturur.
Asitlerin ve Bazların Özellikleri Özellikleri
- Asitlerin tadı ekşidir.
- Asitler aşındırıcı özelliğe sahiptir.
- Asitler bazlarla tepkimeye girdiğinde sonuçta tuz bileşiği ve su oluşur.
- Bazlar kayganlık hissi verir.
pH Skalası Nedir?
Asitlik derecesi ise pH değeri ile ölçülür. pH değeri 7’nin altında olan çözeltiler asidik, 7’nin üzerinde olan çözeltiler bazik olarak tanımlanır. pH değeri 7 olan çözeltiler ise nötrdür.

PytyCzech / iStock
pH, çözeltinin birim hacmindeki artı yüklü hidrojen iyonlarının mol sayısının logaritmasının eksi değeri alınarak hesaplanır. Bir çözeltinin asidik mi, bazik mi olduğu suya göre kıyaslanarak belirlenir. Bu nedenle saf suyun pH değeri 7’ye eşittir yani su nötr bir çözeltidir.
pH=7 Değeri Neden Nötr Kabul Edilir?
Saf su iyonlaşarak artı yüklü hidrojen iyonlarına ve eksi yüklü hidroksil iyonlarına ayrışır.
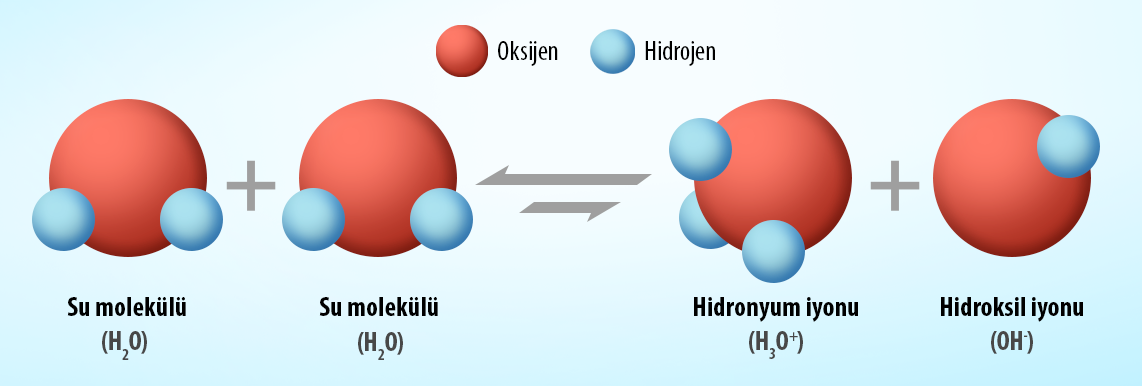
Ancak su moleküllerinin çok küçük bir kısmı ayrışır. Örneğin bir litre suda 1x10-7 mol artı yüklü hidrojen iyonu ve 1x10-7 mol eksi yüklü hidroksil iyonu bulunur. pH değerini hesaplamak için kullanılan formülde hidrojen iyonu derişimi yerine bu değeri koyarak hesaplama yaparsanız pH değerinin 7 olduğunu görebilirsiniz.
Kuvvetli Asit ve Kuvvetli Baz Nedir?
Kuvvetli asitler suda neredeyse tamamen iyonlaşan asitlerdir. Sülfürik asit (H2SO4), hidroklorik asit (HCl), nitrik asit (HNO3), perklorik asit (HClO4) en yaygın bilinen kuvvetli asitlerden bazılarıdır.
Kuvvetli bazlar suda neredeyse tamamen iyonlaşan bazlardır. Sodyum hidroksit en bilinen kuvvetli bazdır.
Zayıf Asit ve Zayıf Baz Nedir?
Zayıf asitler suda kısmen iyonlaşan asitlerdir. Bu nedenle suda çözündüklerinde çözeltiye verdikleri artı yüklü hidrojen iyonu (H3O+) miktarı düşüktür. Sirke asiti olarak bilinen asetik asit, karıncaların ısırdıkları yerin acımasına neden olan formik asit, gazlı içeceklerde bulunan karbonik asit, portakala ekşi tadını veren sitrik asit en bilinen zayıf asitlerden bazılarıdır.
Zayıf bazlar suda kısmen iyonlaşan bazlardır. Bu nedenle suda çözündüklerinde çözeltiye verdikleri eksi yüklü hidroksil (OH-) iyonu miktarı düşüktür. Amonyak en yaygın bilinen zayıf bazlardan biridir.
Kaynaklar:
- https://edu.rsc.org/cpd/acids-and-bases/2000001.article
- https://www.snexplores.org/article/explainer-what-are-acids-and-bases
- https://chemed.chem.purdue.edu/genchem/topicreview/bp/ch11/acidbase.php
- https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_(Physical_and_Theoretical_Chemistry)/Acids_and_Bases/Acid/Overview_of_Acids_and_Bases