Yeni Nesil Alzheimer İlaç Adaylarının Keşfi
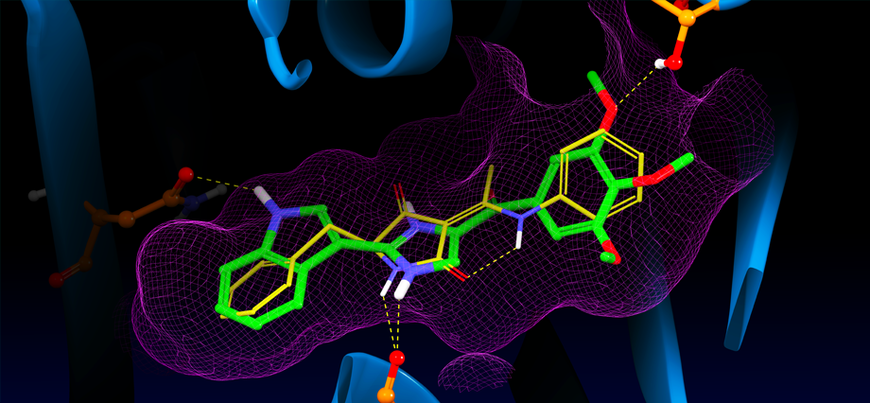
Alzheimer hastalığına neden olan temel faktörlerden olmasına rağmen literatürde β-sekretaz hedefli bir ilaç bulunmamaktadır ve asetilkolinesteraz hedefli ilaçlar da yeterli etki göstermemektedir.
Bu proje kapsamında, Schrödinger’e ait moleküler modelleme paketi olan Maestro yardımıyla standart Alzheimer ilaçlarından daha etkin olabilecek β-sekretaz ve asetilkolinesteraz hedeflerinde yüksek bağlanma afinitelerine sahip ilaç adayları keşfetmeyi amaçladık. Bu amaçla öncelikle günümüzde Alzheimer hastalarında kullanılan 4 farklı ilacın hem β-sekretaz hem de asetilkolinesteraz enzimlerinde bağlanma afinitelerini ölçtük. Böylelikle bu iki hedef proteinin aktif bölgelerine bağlanacak küçük moleküllerin bağlanma enerjisi için referans değerleri tahmin etmiş olduk. Bu referans verileri göz önüne alınarak dış küçük molekül data banklardan (örneğin ZINC) hazır (sentezlenmiş) moleküller ile De Novo molekül tasarım yöntemleriyle türetilen yeni molekülleri karşılaştırdık. Bağlanma afinitesi standart ilaçlara (referans değerler) göre daha iyi sonuç veren molekülleri bir sonraki aşama için düşünürken, standart ilaçlardan kötü bağlanma afinitesine sahip molekülleri elimine ettik.
De Novo işlemi ile yeni tasarlanan 5719 farklı liganddan 134 tanesinin başlangıç (referans) durumuna göre daha düşük enerjili olduğu ve bunların da 15 tanesinin ilaç olarak geliştirilmesi için uygun olduğunu belirledik. Sonuç olarak yeni elde edilen ilaçların bağlanma enerjilerinin, referans alınan ilaçlara göre daha düşük enerjili olduğunu gördük. Projenin ilerleyen aşamalarında ilaç olma potansiyeline sahip olan ilaçların sentezleme aşamalarını gerçekleştireceğiz.
Giriş
Alzheimer Hastalığı; beynin, öncelikle hafıza olmak üzere, tüm bilişsel fonksiyonlarında ilerleyici kayba neden olan ve mikroskopik olarak beyinde anormal protein depolanmasıyla karakterize bir hastalığıdır. Halk arasında “bunama” olarak bilinen “demans”; “hafıza, lisan, aritmetik, karar verme yetisi, dikkat ve diğer bilişsel fonksiyonlarda ilerleyici kayıp” demektir. Her Alzheimer hastası demanslıdırama, her demans hastası Alzheimer hastası değildir. Çünkü,demansa neden olan onlarca başka hastalık vardır. Alzheimer Hastalığı ise, en sık görülen demans tipidir. Bu nedenle sıklıkla ve kimi zaman yanlışlıkla, Alzheimer hastalığı ile demans terimleri birbiri yerine kullanılmaktadır.
Alzheimer hastalığı (AH), bunama yapan hastalıklar içinde en sık izlenen bozukluktur. AH yeni bir hastalık olmasa da hastaların sayısı giderek artmaktadır. Çünkü Alzheimer ile ilgili en önemli risk faktörü yaştır ve yaşlanma kaçınılmaz bir durumdur. Günümüzde tüm dünyada (özellikle gelişmiş ülkelerde ve refah toplumlarında) en hızlı artan yaş grubunu 65 yaş ve üstü kişiler oluşturmaktadır. Alzheimer hastalığının görülme sıklığı yaş ile artmaktadır (65 yaş üstü 100 kişiden 8'inde Alzheimer hastalığı görülmektedir). 21. yüzyılda doğal, sosyal veya ekonomik felaketlerle karşılaşılmazsa hastalığın görülme sıklığı daha da artacaktır. Günümüzde Türkiye’de 300 bin civarında Alzheimer hastası olduğu düşünülmektedir. Genç nüfusun giderek yaşlanacağı bir ülke olarak Türkiye’de 30-40 yıl sonra bu hastalığın en önemli sağlık sorunu olacağı ön görülmektedir.
Amacı
Insiliko teknikler, laboratuvar ortamında günler alan işlemleri bilgisayar ortamında dakikalara indirgeyen yeni nesil çalışma yöntemlerinden biridir.
Bu teknikler kullanılarak yapılan ilaç tasarım çalışmaları ilaç etken maddesi sentezlenmeden, biyoaktivitesi hakkında bilgi edinmeyi sağlar. Böylece zamandan ve maddi kaynaklardan tasarruf sağlanır.
Alzheimer hastalığına yakalananların sayısının artmasına ve geleceğin en önemli sağlık problemleri arasında görülmesine karşın henüz kesin bir tedavi yöntemi bulunmamaktadır. Hasta yakınlarının desteği ve çeşitli ilaç tedavileri ile Alzheimer hastalığı geciktirilebilir fakat günümüzdeki koşullara bakıldığında Alzheimer hastalığının tamamen ortadan kaldırılması veya engellenmesi söz konusu değildir.
Piyasada NMDA(N-metil D-aspartat) reseptör antogonistleri ve asetilkolin esteraz inhibitörleri adı altında çeşitli ilaçlar bulunmakla birlikte β-sekretaz (Alzheimer’a neden olan bir çeşit enzim) hedefli herhangi bir ilaç bulunmamaktadır. Bu proje kapsamında, Schrodinger’e ait moleküler modelleme paketi olan Maestro yardımıyla standart Alzheimer ilaçları dışında bulduğumuz farklı molekülleri β-sekretaz proteinine bağlayarak piyasadaki ilaçlardan daha iyi sonuçlarda moleküller bulmayı ve bu moleküllerde bağlanmayan bölgelerle kendi veritabanımızda olan kısımları değiştirerek piyasadaki ilaçlardan daha iyi bağlanma enerjileri olan, β-sekretaz proteini üzerinde daha büyük etki yaratan ilaçlar tasarlamayı amaçladık.
Yöntem
Proje süresince Ligand Preparation ve ligand docking işlemlerini Intel Xeon(R) CPU ES-2670 v2 2.50 GHz ve Intel Core i53470S CPU 2.90GHz özelliklerindeki bilgisayarlarda, DeNovo işlemi ise Intel Core i53470S CPU 2.90GHz özelliklerindeki is istasyonlarında Schrodinger Maestro v9.3.5 programıyla Linux platformunda gerçekleştirdik.
Projeyi temel olarak dört basamakta yürüttük.
1. Referans Alınacak Sonuçaların Belirlenmesi
2. Ligand Kenetleme İşlemleri
3. Asetilkolinesteraz İncelenmesi
4. De Novo Çalışmaları
1. Aşama: Referans Alınacak Sonuçların Belirlenmesi
Alzheimer hastalığının tedavisinde kullanılan asetilkolinesteraz hedefli ilaçlar Donepezil, Galantamin, rivastigmin ve takrin olmak üzere 4 adetti. Bu ilaçların 2D yapıdaki moleküler çizimlerini yaptık ve sanal ortama aktaardık. Molekülü hidrofilik, hidrofobik etkileşimler, van der Walls ve hidrojen bağlarına göre düşük enerjiye ulaştıracak şekilde hazırlayan Ligand Preparation işlemiyle moleküllerin 3D yapılarını elde ettik.
Alzheimer’a neden olan ve amiloid plak oluşumunda etkili olan Protein Data Bank’tan(PDB) indirdiğimiz 1W51 PDB kodlu β-sekretaz proteinine hidrojen ekleme, eksik yan zincirleri tamamlama gibi Protein Preparation işlemleri uygulanarak eksiklik ve hatalarını giderdik. Grid Generation işlemi ile moleküllerin protein üzerinde hedeflendirileceği aktif bölgeyi saptadık.
Projede kullandığımız moleküler kenetleme yöntemi olan Glide Docking’te kullanılan üç yöntem vardır. HTVS (High-Throughput Virtual Screening) aralarında en hızlı olanı fakat doğruluk payı en düşük olan yöntem, SP (Standard Precision) ortalama hız ve doğruluk payına sahip olan yöntem, XP (Extra Precision) doğruluk payı en yüksek olan yöntemdir.
Ligand Preparation ile hazırlanan dört adet ilacın herbirini β-sekretaz proteinine Glide/HTVS, Glide/SP ve Glide/XP kullanarak bağladık. Bu işlemler sonucunda elde ettiğimiz docking skorları, projenin ilerleyen aşamalarında ilaç adayı olarak belirleyeceğimiz ligandları seçmede referans değer olarak kullandık.
2. Aşama: Ligand Kenetleme İşlemleri
Projede taranacak moleküller geniş bir molekül veri tabanı olan ZINC database kullanarak indirdik ve Maestro’ya iki boyutlu olarak aktardık. İndirdiğimiz yaklaşık 4 milyon molekülü Ligand Preparation işlemleriyle docking için haır ligandlar haline getirdik.
Hazırladığımız ligandların her birini, projenin ilk aşamalarında düzenlediğimiz reseptör proteine (BACE1) bağladık. Sırasıyla Glide/HTVS, Glide/SP ve Glide/XP ve in siliko ve statik ortamda en doğru sonuçları veren IFD (Induced Fit Docking) işlemi uyguladığımız ligandlardan, referans skor olan -10.0 kcal/mol’den daha iyi bağlanma skoru gösterenler yani daha düşük enerji ile bağlananları seçerek her bir basamakta ligand sayısını azalttık.
3. Aşama: Asetilkolinesteraz İncelenmesi
Alzheimer Hastalığına neden olan bir başka enzim asetilkolinesteraz olması ve standart ilaçların asetilkolinestraz hedefli olması nedenleriyle proje kapsamında asetilkolinesterazın da incelememiz gerektiğini düşündük. 4TVK PDB kodlu AChE (Asetilkolinesteraz) proteinine Protein Preparation Wizard işlemi uygulayarak eksiklik ve hatalarını düzelttik.
BACE1 proteinine de bağladığımız olan dört adet ilacın herbirini 4TVK kodlu reseptöre Glide/HTVS, Glide/SP ve Glide/XP kullanarak bağladık. Daha önceden ZINC database’den indirdiğimiz ve ligand hazırlama işlemlerini yaptığımız ligandları, düzenlemiş olduğumuz hedef proteine (AChE) Glide Docking işlemiyle bağladık.
4. Aşama: De Novo Çalışmaları
Başlangıçta bulunan yaklaşık 4 milyon ligand içinden seçtiğimiz en iyi 4 ligandın 2D ve 3D diyagramlarını inceledik. Kenetleme işleminde pasif kalan, yani aktif bölge ile herhangi bir etkileşim göstermeyen kısımları belirledik. Daha sonra bu kısımlara Combi Glide işleminin bir alt ürünü olan DeNovo işlemini uyguladık. Bu işleme göre aktif olmayan kısımları çıkartarak yerine elimizde bulunan 43 adet farklı küçük organik fragment ekledik. Sonucunda 5719 farklı kombinasyon elde ettik. Bu elde edilen 5719 adet farklı ligandı, ligand kenetleme işlemleri uygulayarak proteinin aktif bölgesinde taradık.
Sonuç ve Tartışma
Proje süresince hedefimiz standart Alzheimer ilaçlarından daha etkin olabilecek ilaç adayları bulmaktı. Bu hedefimiz doğrultusunda ligand docking işlemleri sonucunda, sentezlenmiş olarak bulunan ve farklı amaçlar için kullanılan 14 adet küçük molekülün Alzheimer hastalığı üzerinde de etkili olduğunu keşfettik. Bunun yanında keşfettiğimiz moleküllerin değerlerini iyileştirmek için yaptığımız De Novo işlemi sonucunda 15 adet yeni ilaç adayları tasarladık.
Beta sekretaz hedefli, en iyi olarak belirlediğimiz 14 molekül içinden 3 tanesini Chembridge Corp. dan sipariş ettik. Sipariş edilen moleküllerin İn Vitro deneyleri Ağrı İbrahim Çeçen Üniversitesi Biyokimya Bölümünden Doç. Dr. Murat Şentürk tarafından gerçekleştirildi. Sipariş edilen 3 molekülün asetilkolinesteraz deneyleri yapıldı. Aslında beta sekretaz hedefli olan bu moleküller asetilkolinesteraz üzerinde de standart Alzheimer ilaçları kadar iyi etki gösterdi. (Beta sekretaz üzerinde standart ilaçlardan çok daha iyi inhibe edici etki göstermektedirler.) Standart Alzheimer ilaçları sadece asetilkolinesteraz hedefli iken bizim bulduğumuz moleküller iki protein üzerinde de çok iyi inhibe edici etki göstermektedirler.
Farklı amaçlar için kullanılan kimyasalların Alzheimer tedavisinde ilaç olarak kullanılabileceğini bulmanın yanında bu ilaçları daha da geliştirdik. Projenin ilerleyen aşamalarında ise nihai hedefimiz yeni tasarladığımız molekülleri sentezleyerek kendi ilacımızı üretmektir.
Kaynaklar
1. Ergün U, "Alzheimer nedir?", Türk Geriatri Derneği (http://www.turkgeriatri.org/sorulariniza_yanitlar.php?pg=alzheimer)
2. "Alzheimer Hastalığı", Türk Nöroloji Derneği. (http://www.noroloji.org.tr/page.aspx?menu=473)
3. Bettens, K. ve ark., "Current status on Alzheimer’s disease molecular genetics: from past, to present, to future", Hum Mol Genet, 19, R4-R11, 2010.
4. Selkoe, D.J., "Alzheimer’s disease: Genes, proteins, and therapy", Physiological Reviews, 81, 701-66, 2001.
5. Saka, E., "Pathophsiology of Alzheimer's Disease: Experimental and genetics findings", Turkish Journal of Geriatrics, 3, 21-26, 2010.
6. Strittmatter, W.J. ve ark., "Apolipoprotein E: high avidity binding to beta-amyloid and increased frequency of type 4 allele in late-onset familial AD", Proc Natl Acad Sci, 90:1977-1981, 1993.
7. Corder, E.H., ve ark., "Gene dose of apolipoprotein E type 4 allelle and the risk of Alzheimer’s disesase in late onset families", Science, 261, 921-923, 1993.
8. Roses, A.D., "Apolipoprotein E alleles as risk factors in Alzheimer’s disease", Annu Rev Med, 47, 387-400, 1996.
9. Kim, J. ve ark., "The Role of apolipoprotein E in Alzheimer’s Disease", Neuron, 63, 287-303, 2009.
10. Yalgın, Ç., "Alzheimer hastalığında kolinomimetik tedavis", 2009. (http://www.bilimfeneri.gen.tr/kitaplik/pdf/kolinomimetik.pdf)
11. Meraz-Rios, M. A. , ve ark., "Tau oligomers and aggregation in Alzheimer’s disease". J Neurochem, 112, 1353-1367, 2010.
12. Ludolph, A.C. ve ark., "Reisenburg Working Group for Taupathies with Parkinsonis. Taupathies with parkinsonism: clinical spectrum, neuropathologic basis, biological markers, and treatment options", Eur J Neurol, 16, 297-309, 2009.
13. Haass, C., Selkoe, D.J., "Soluble protein oligomers in neurodegeneration: lessons from the Alzheimer’s amyloid β-peptide", Nature reviews, 8, 101-112, 2007.
14. http://www.beyin-beyin.com/norotransmitterler/
15. Alzheimer's Disease Education and Referral Center, a service of the National Institute on Aging.
16. Kürtüncü M, "Alzheimer Hastalığı", 2012. (http://www.norolojiklinigi.info/alzheimer_hastaligi.html)
17. LigPrep, version 2.5, Schrödinger, LLC, New York, NY, 2012.
18. Schrödinger Suite 2012 Protein Preparation Wizard; epik version 2.3, Schrödinger, LLC, New York, NY, 2012, Impact version 5.8, Schrödinger, LLC, New York, NY, 2012; Prime version 3.1, Schrödinger, LLC, New York, NY, 20
19. Glide, version 5.8, Schrödinger, LLC, New York, NY, 2012.
20. Induced Fit, version 5.8, Schrödinger, LLC, New York, NY, 2012.
21. The Alzheimer's Association, Alzheimer's disease facts and figures, 2010.
Ekip Tanıtımı
Merve Sevinç
Adım Merve Sevinç. 17 yaşındayım. Aslında Kocaeli'de oturuyorum fakat İstanbul Atatürk Fen Lisesine gitttiğim için yurtta kalıyorum. Lisanslı voleybolcu ve okçuyum. Aynı zamanda resim çizmeyi, müzik dinlemeyi ve yan flüt çalmayı seviyorum. Matematik, biyoloji ve kimya ile ilgilenmeyi seviyorum. Bu yüzden okulun biyolji olimpiyat takımına girdim. Sonra ise Aslı ile tanıştım ve beraber kimya projesi hazırlamaya başladık. İleride bir bilimadamı hekim olmak istiyorum. Çünkü doktor olmak her zaman hayalimdir daha doktorluk dışında hiçbir mesleği seçmeyi düşünmedim. Ama aynı zamanda araştırmaya ve bilime de büyük ilgim var. bu yüzden bilimadamı hekim olmak bence harika bir fikir.
Aslu Ustabaş
Adım Aslı Ustabaş. İstanbul Atatürk Fen Lisesinde okuyorum. Ama ailem Düzce'de yaşıyor. Lise için ailemden ayrılmak çok zor bir karar oldu. Ama bir fen lisesinde okumak istiyordum. Küçüklüğümden beri bilime karşı ilgiliydim. Hatta ilk oyuncağım matematikle ilgiliydi. Bu ilgimi lisedeykende devam ettirdim ve okulun biyoloji ve matematik takımlarına girdim. Daha sonra Merve ile tanıştım ve beraber çalışmaya başladık.