Çözünme Nasıl Gerçekleşir?
Deneyler köşesinin bu projesinde, tuz ve aspirinin çözünme süreçlerini karşılaştırarak çözünme ve kristalleşme olaylarını inceliyoruz.

ttsz / iStock
Bilmekte Fayda Var!
Suya şeker ekleyip karıştırdığımızda şekerin suda eridiğini söyleriz. Aslında şeker gerçekten suyun içinde erimez. Tanık olduğumuz olay aslında bir çözünmedir. Şeker molekülleri su moleküllerinin arasında homojen bir şekilde dağılarak çözelti oluşturur.
Çözünme Nedir, Nasıl Gerçekleşir?
Katı, sıvı ya da gaz hâlindeki bir maddenin bir çözücü içinde homojen bir şekilde dağılarak çözelti oluşturmasına çözünme denir. Çözünme sırasında çözünen madde iyon ya da moleküllerine ayrışır ve her iyon ya da molekülün etrafı çözücü molekülleri tarafından sarılır.
Çözünme olayının nasıl gerçekleştiğini anlayabilmek için moleküler seviyedeki etkileşimleri incelememiz gerekir.
Neden Yağ Suyun İçinde Çözünmez?
Bir maddenin başka bir madde içinde çözünebilmesi için çözünen maddenin molekülleri ile çözücü maddenin moleküllerinin birbiriyle etkileşim kurması gerekir. Bu nedenle çözünmenin gerçekleşmesinde moleküllerin özellikleri ve moleküller arasındaki etkileşimler önemlidir.
Polar Molekül Nedir?
Su molekülü bir oksijen atomuna bağlı iki hidrojen atomundan oluşur. Su molekülü polar bir moleküldür. Suyu oluşturan hidrojen ve oksijen atomlarının elektronegatiflikleri yani bağ oluşumunda yer alan elektronları çekme istekleri birbirinden farklıdır. Oksijenin elektronegatifliği hidrojeninkinden daha yüksek olduğu için oksijen atomu oksijen bağ oluşumunda yer alan elektronları hidrojene kıyasla daha fazla çeker. Bu nedenle oksijen atomunun üzerindeki eksi yük yoğunluğu hidrojen atomlarının üzerindekinden daha yüksektir. Sonuçta su moleküllerindeki oksijen atomları kısmen negatif, hidrojen atomu ise kısmen pozitif yüke sahip olur. Bu tür moleküller polar olarak isimlendirilir.
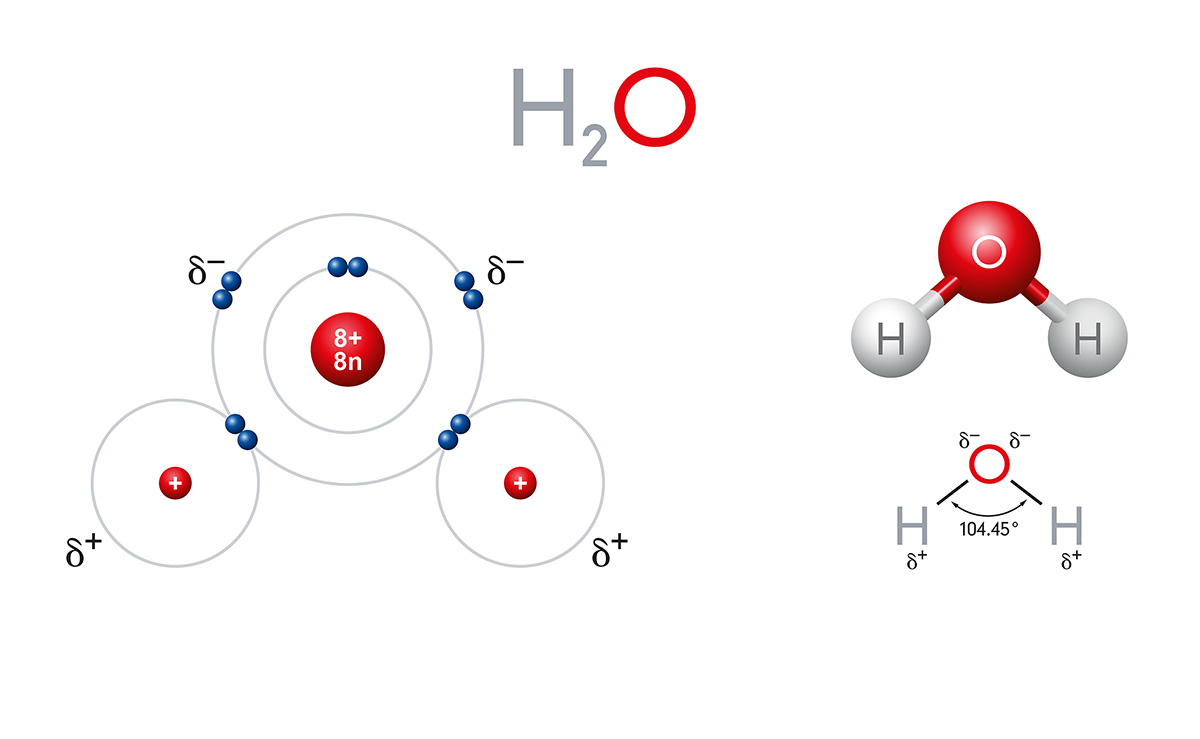
Peter Hermes Furian/Alamy Stock Photo
Su molekülü (H2O), bir oksijen ve iki oksijen atomundan oluşur. Su moleküllerindeki oksijen atomları kısmen negatif, hidrojen atomu ise kısmen pozitif yüke sahiptir.
Hidrojen Bağı Nedir?
Su molekülündeki bu yük dağılımı nedeniyle bir su molekülünün kısmen eksi yüklü oksijen atomu ve diğer bir su molekülünün artı yüklü hidrojen atomu arasında elektriksel bir çekim kuvveti ortaya çıkar. Bu etkileşim hidrojen bağı olarak isimlendirilir.
Apolar Molekül Nedir?
Yağ molekülünün içindeki yükler ise dengeli bir şekilde dağılır. Bu tür moleküller polar olmayan yani apolar olarak adlandırılır.
Bu durumda yağ molekülleri su moleküllerine göre birbirlerine daha yakın olur. Su molekülleri de birbirlerine daha çok çekim uyguladığından su ve yağ molekülleri birbirine karışmaz.
Şekerin Yapısı ve Özellikleri
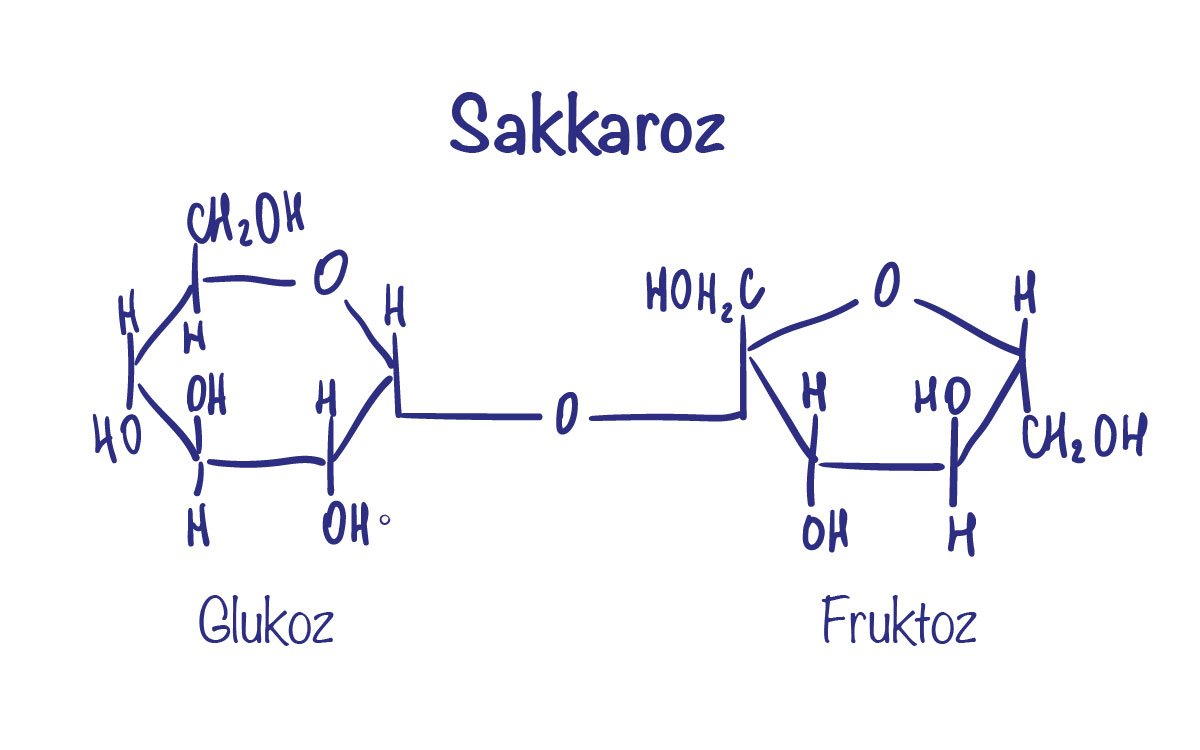
Tetiana Kovalenko/Alamy Stock Vector
Sofra şekeri olarak bildiğimiz sakkaroz, glikoz ve fruktoz moleküllerinin birbirine bağlanmasıyla oluşur.
Şeker, sakkaroz adı verilen moleküllerden oluşur ve katı hâlde kristal yapıdadır. Şeker suyun içine karıştırıldığında şeker kristalindeki sakkaroz molekülleri birbirinden ayrılır. Sakkaroz polar bir molekül olduğundan sakkaroz molekülündeki kısmen eksi yüklü kısımlar su molekülündeki kısmen artı yüklü kısımlar tarafından, sakkaroz molekülündeki kısmen artı yüklü kısımlar ise su molekülündeki kısmen eksi yüklü kısımlar tarafından çekilir. Bu etkileşim şekerin suda çözünmesini sağlar. Ancak sakkaroz molekülünü oluşturan atomlar arasındaki kovalent bağlar kopmaz. Yani suda çözünen sakkaroz molekülleri, tek bir molekül olarak suyun içinde dağılır.
Deneyler köşesinin bu projesinde, tuz ve aspirinin çözünme süreçlerini karşılaştırıp çözünme ve kristalleşme olaylarını inceliyoruz.
Nelere İhtiyacımız Var?
- Aspirin
- Tuz
- Kolonya
- Su
- Mikroskop
- Lam
- Damlalık
- Bardak
- Çay kaşığı
Ne Yapıyoruz?
- Bir adet aspirin tabletini toz hâline gelinceye kadar ezelim.
- 4 tane bardak alalım. Bardaklardan ikisinin içine toz hâline getirdiğimiz aspirinden eşit miktarda ekleyelim.
- Diğer iki bardağın her birine çay kaşığının üçte biri kadar tuz ekleyelim.
- Aspirin koyduğumuz bardaklardan biri ile tuz koyduğumuz bardaklardan birine beşer çay kaşığı su ekleyip karıştıralım.
- Aspirin koyduğumuz diğer bardak ile tuz koyduğumuz ikinci bardağa beşer çay kaşığı kolonya ekleyip karıştıralım.
- Hazırladığımız aspirin-kolonya karışımından çok az miktarda alarak lamın üzerine yerleştirelim ve mikroskopta 10 kat büyüterek inceleyelim.
- Bardaklarda kalan su ve kolonya buharlaşana kadar bekleyelim.
Ne Oldu?
Aspirini ve tuzu ayrı ayrı hem su hem kolonya ile karıştırdık. Sonuçta aspirinin kolonyanın, tuzun ise suyun içinde daha iyi çözündüğünü gözlemledik.
Hazırladığımız karışımlardaki su ve kolonyayı buharlaştırdığımızda, tuz-su çözeltisindeki tuzun ve aspirin-kolonya çözeltisindeki aspirinin tekrar kristal oluşturduğunu gördük.

Tuz kristalleri
Aspirin-su ve tuz-kolonya karışımlarında ise çok fazla kristalleşme olmadı.
Mikroskopta incelemek amacıyla aspirin-kolonya çözeltisinden lamın üzerine koyduğumuzda etil alkol hızlıca buharlaştı. Çünkü etil alkol kolay buharlaşabilen bir maddedir.
Aspirin-kolonya çözeltisini bir süre beklettiğimizde oluşan kristaller ile hızlı buharlaşma sonucu oluşan aspirin kristalleri arasında bazı şekil farklılıkları olduğunu gördük.
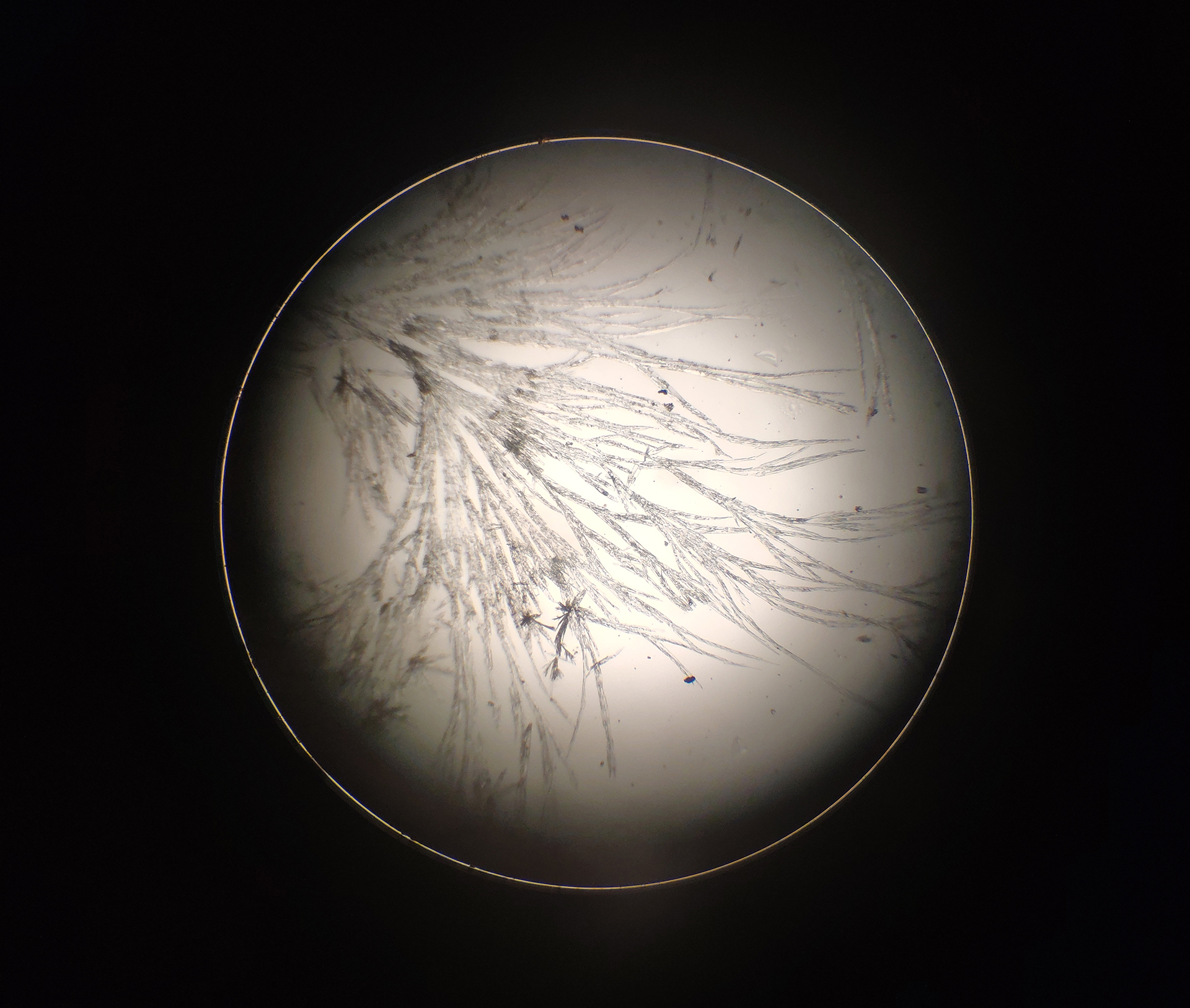
Hızlı buharlaşma sonucu oluşan aspirin kristalleri
Hızlı buharlaşma sonucu oluşan aspirin kristalleri dallanmış fraktal yapılar oluştururken, yavaş buharlaşma sonucu oluşan aspirin kristalleri ise daha büyük ve dikdörtgen şekilli yapılar oluşturdu.
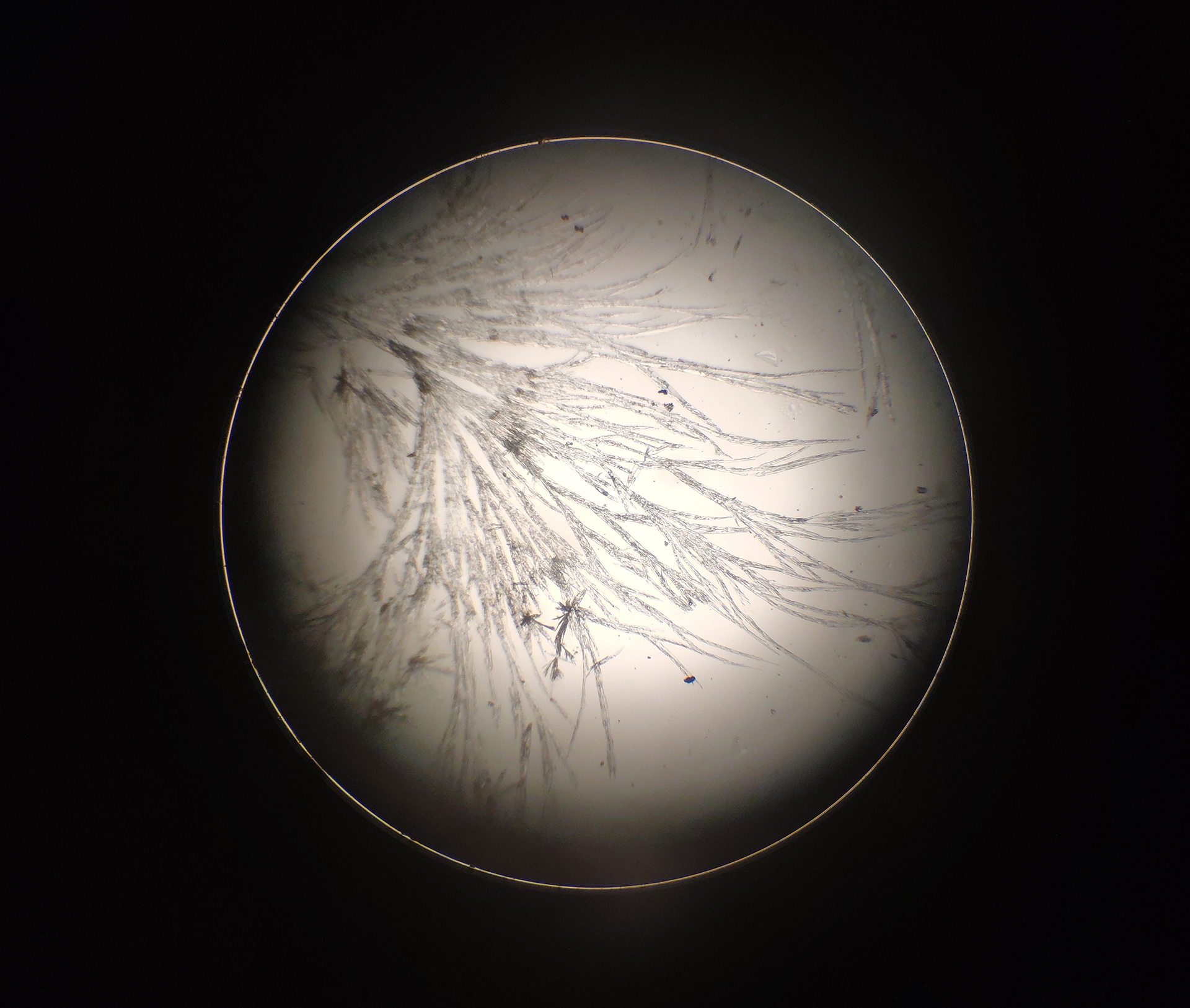
Yavaş buharlaşma sonucu oluşan aspirin kristalleri
Aspirin, asetilsalisilik asit isimli kimyasal bir maddeden oluşur.
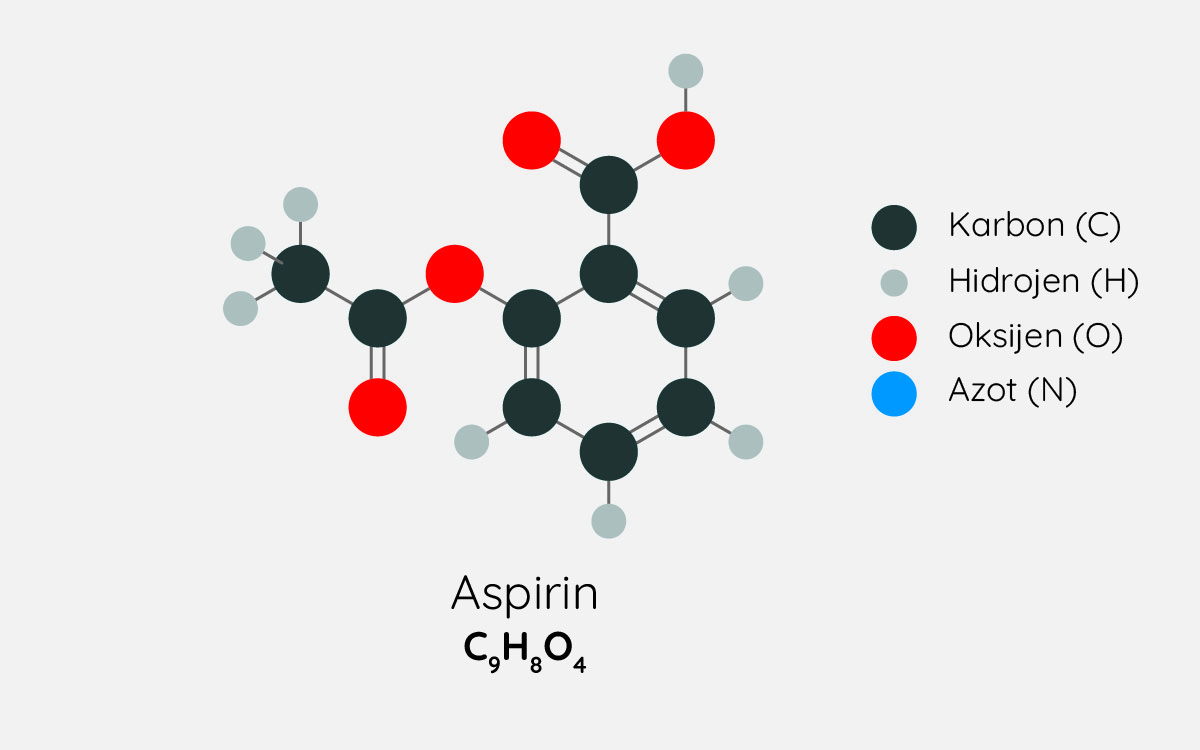
jack0m/iStock
Aspirinin (asetilsalisilik asit) kimyasal yapısı
Aspirin, büyük oranda etil alkol içeren kolonyanın içinde çözündü. Bunun sebebini anlayabilmek için aspirinin yapısı hakkında bilgi sahibi olmamız gerekiyor.
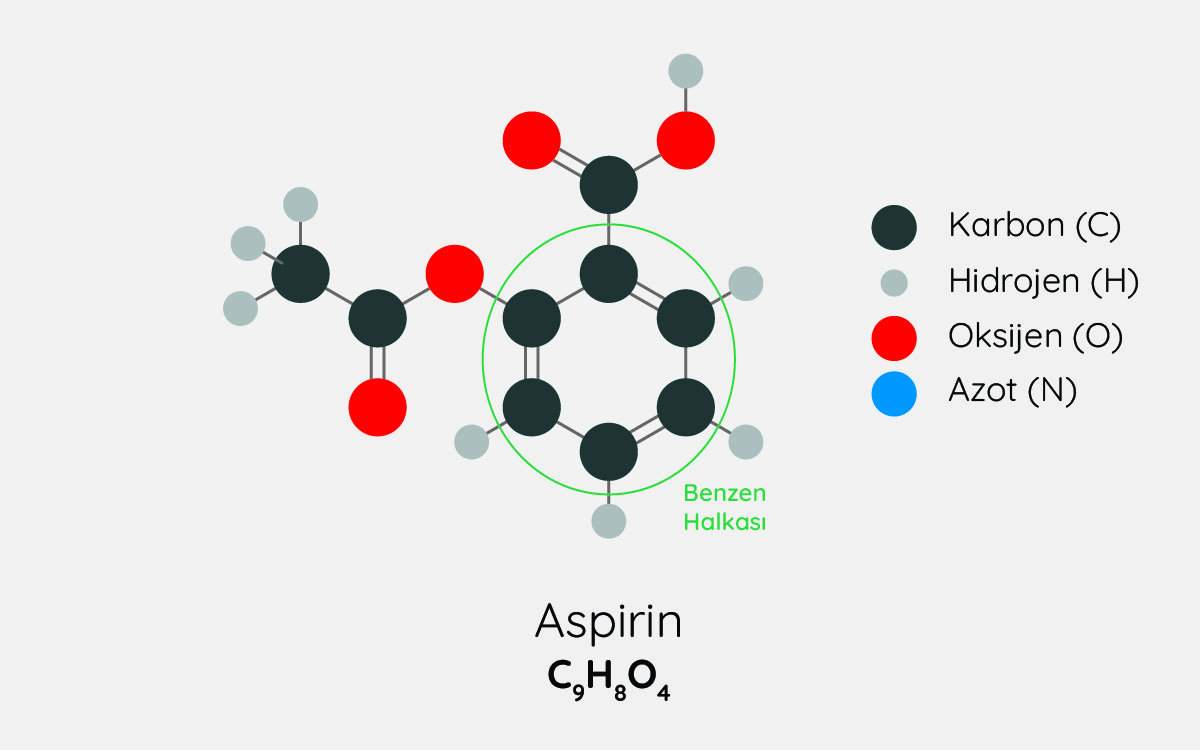
jack0m/iStock
Aspirin molekülündeki benzen halkası apolar yapıdadır.
Şekildeki bölüm benzen halkası olarak adlandırılır. Bu grupta elektriksel yük dağılımı dengeli olduğu için benzen halkası apolar yapıdadır.
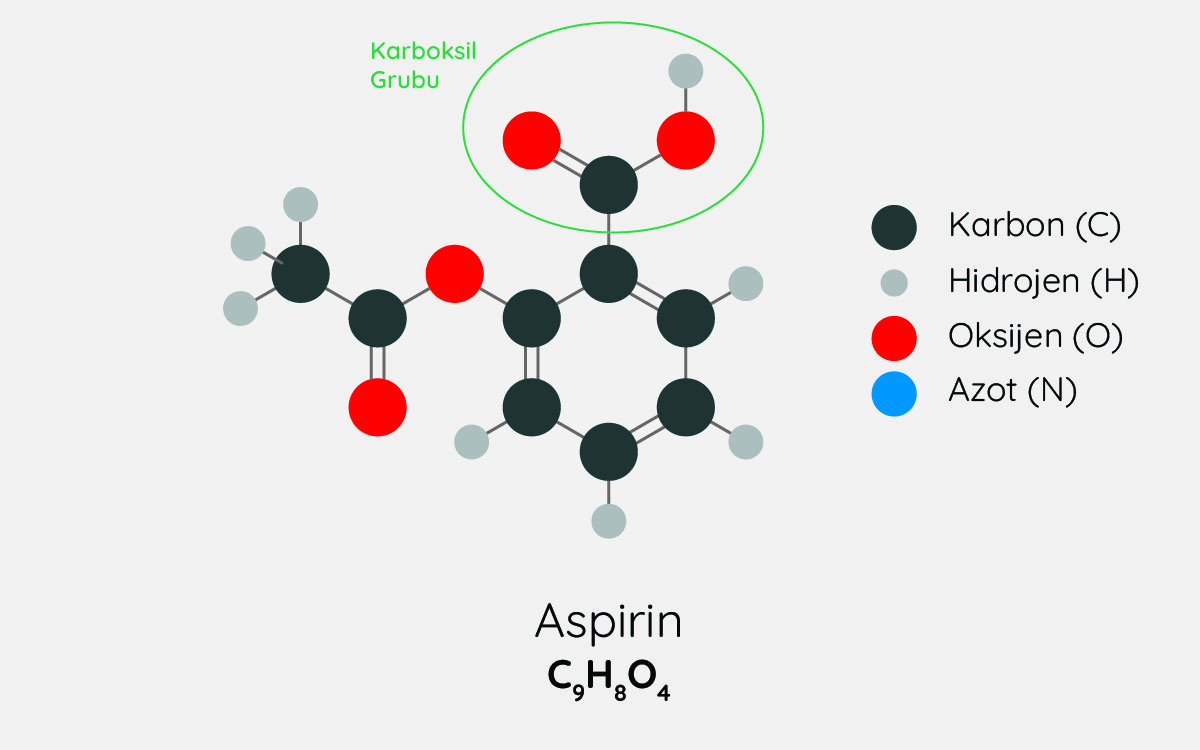
jack0m/iStock
Aspirin molekülündeki karboksil grubu polar yapıdadır.
Şekildeki bölüm karboksil grubudur. Bu grupta elektriksel yük dağılımı dengeli olmadığı için karboksil grubu polar yapıdadır.

jack0m / iStock
Aspirin molekülündeki metin ester grubu polar yapıdadır.
Şekildeki bölüm metil ester grubudur. Bu grupta elektriksel yük dağılımı dengeli olmadığı için metil ester grubu polar yapıdadır.
Su polar yapıda bir çözücü olduğundan aspirinin yapısındaki karboksil grubu ve metil ester grubu ile etkileşir. Ancak benzen halkası polar olmadığı için su bu kısım ile etkileşemez.
Kolonya ise büyük oranda etil alkol içerir. Etil alkolün yapısı aşağıdaki gibidir.
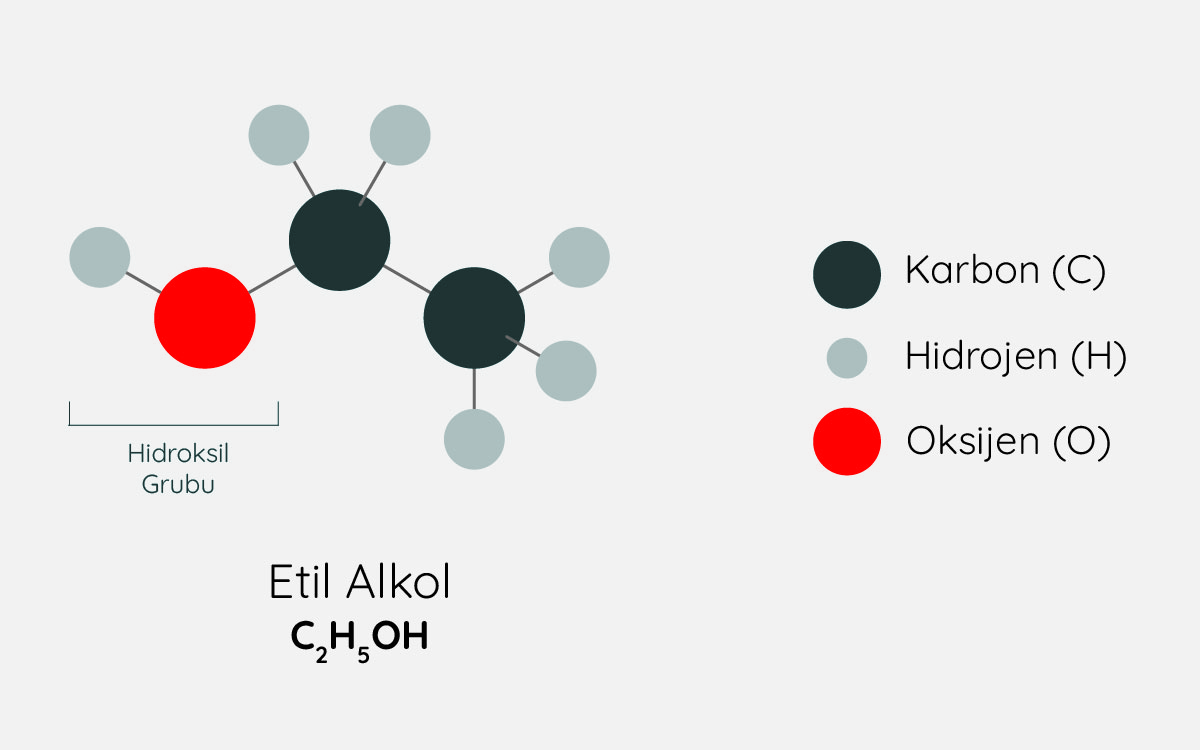
jack0m/iStock
Etil alkolün kimyasal yapısı.
Etil alkoldeki hidroksil grubu polar yapıdayken, molekülün diğer bölümleri apolar yapıdadır. Bu sayede etil alkolün polar grubu aspirindeki polar bölümleri çözerken, etil alkoldeki polar olmayan bölüm aspirindeki polar olmayan bölümleri çözer. Sonuçta aspirin, etil alkolde sudakine göre daha iyi çözünür.
ttsz/iStock
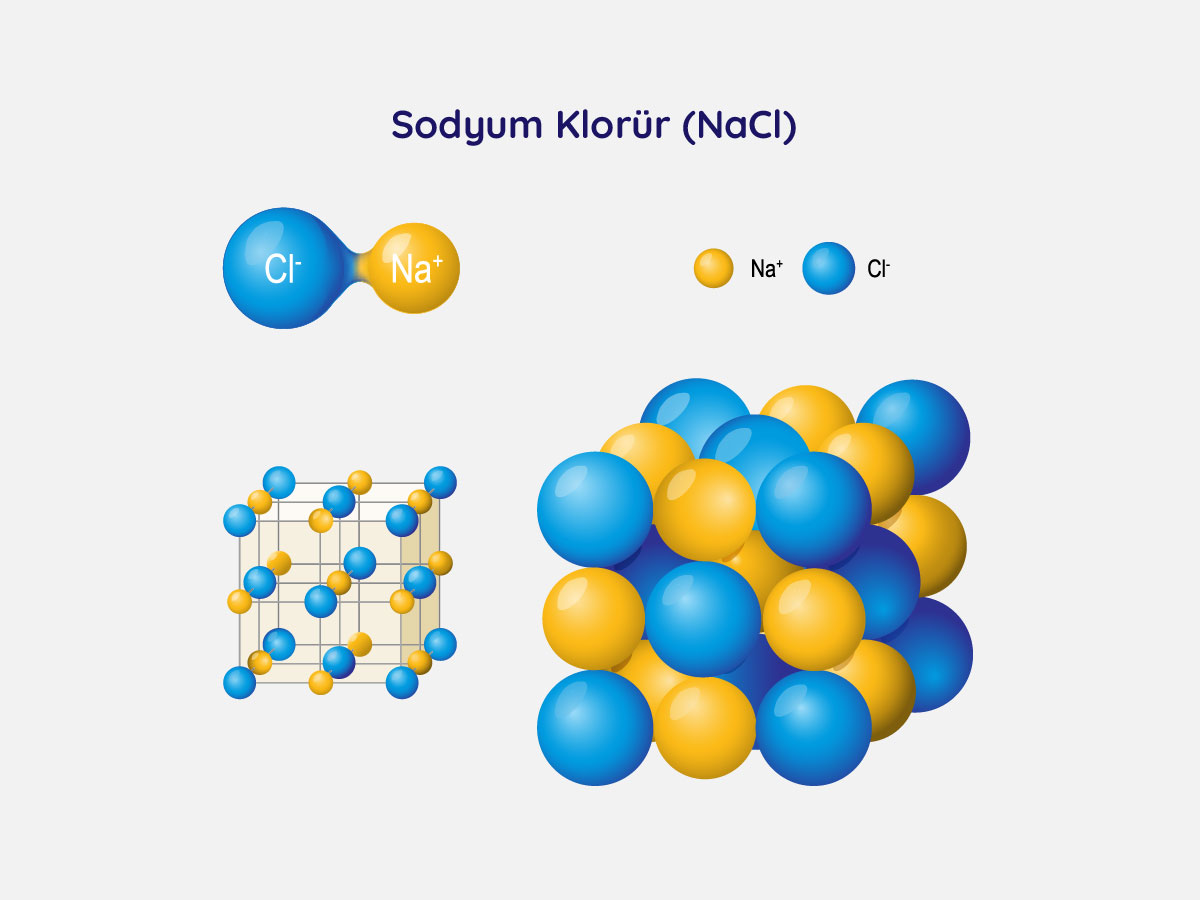
Tuzun kristal yapısı
Sofra tuzu sodyum klorür moleküllerinden oluşur. Bu molekülde sodyum (Na) ve klor (Cl) atomları birbirine iyonik bağ ile bağlıdır. Yani sodyum son enerji seviyesindeki bir elektronu klora vererek sodyum klorür bileşiğini oluşturur. Tuz suda çözündüğünde artı yüklü sodyum iyonları ve eski yüklü klor iyonlarına ayrışır.

ttsz/iStock
Tuz suda nasıl çözünür?
Su moleküllerindeki kısmen eksi yüklü oksijen atomları artı yüklü sodyum iyonlarını sararken, kısmen artı yüklü hidrojen atomları eksi yüklü klor iyonlarını sarar. Böylece tuz suda homojen bir şekilde dağılmış yani çözünmüş olur.
Kaynaklar:
- Ostadhashem, A. H. Ve Peyvandi, K., “Measurement solubility of Acetylsalicylic Acid in water and alcohols.”, International Pharmacy Acta, Cilt 3, Sayı 1, s. 3e11:1-7, 2020.
- https://bilimgenc.tubitak.gov.tr/makale/tuz-suda-nasil-cozunur
- https://steemit.com/zzan/@josalarcon2/science-blog-making-aspirin-crystals
- https://www.usgs.gov/media/images/water-molecules-and-their-interaction-salt
- https://chem.libretexts.org/Bookshelves/Introductory_Chemistry/Basics_of_General_Organic_and_Biological_Chemistry_(Ball_et_al.)/09%3A_Solutions/9.03%3A_The_Dissolution_Process
- https://www.acs.org/content/dam/acsorg/education/k-8/inquiry-in-action/fifth-grade/g5-l2.1-bkgd.pdf
- https://web.fscj.edu/Milczanowski/psc/lect/Ch10/slide10.htm
Yazar Hakkında:
Dr. Sevda Seçer Esmer
İzmir Arkas Bilim ve Sanat Merkezi Fen Bilimleri Öğretmeni















Yorumlar
mikail06 Per, 02/08/2024 - 11:50
Metil alkol ile etil arasında fark nedir?